COVID-19
Pfizer y BioNTech anuncian la primera vacuna fiable contra la COVID-19
Últimos pasos para uno de los proyectos más novedosos de vacuna, basada en el ARNm mensajero sintético del virus
La fase tres del ensayo comenzó el pasado 27 de julio y ha implicado a 43.538 participantes hasta la fecha, de los que 38.955 recibieron la segunda dosis el pasado 8 de noviembre.
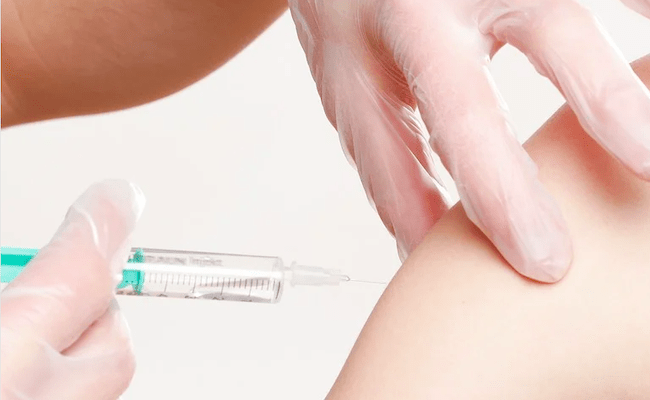
Albert Bourla, presidente y director ejecutivo de Pfizer, ha anunciado una gran noticia para la lucha contra la COVID-19, al compartir que el proyecto de vacuna en el que trabajan, junto con el laboratorio alemán BioNTech, ha ofrecido "resultados positivos de eficacia de nuestro estudio de fase 3, etapa tardía de nuestra posible vacuna COVID-19". “Hoy es un gran día para la ciencia y la humanidad".
“Estamos alcanzando este hito crítico en nuestro programa de desarrollo de vacunas en un momento en el que el mundo más lo necesita, con tasas de infección que establecen nuevos récords, hospitales que se acercan al exceso de capacidad y economías que luchan por reabrir. Con las noticias de hoy, estamos un paso significativo más cerca de brindar a las personas de todo el mundo un avance muy necesario para ayudar a poner fin a esta crisis de salud mundial. Esperamos poder compartir datos adicionales de eficacia y seguridad generados por miles de participantes en las próximas semanas ”. D
Esta candidata a vacuna supera el 90% de efectividad para prevenir COVID-19 en participantes sin evidencia de infección previa por SARS-CoV-2, "en el primer análisis de eficacia provisional". "Los resultados demuestran que nuestra vacuna basada en ARNm puede ayudar a prevenir COVID-19 en la mayoría de las personas que la reciben".
"La división de casos entre las personas vacunadas y las que recibieron el placebo indica una tasa de eficacia de la vacuna superior al 90 %, 7 días después de la segunda dosis. Esto significa que la protección se logra 28 días después del inicio de la vacunación, que consiste en un esquema de 2 dosis. A medida que continúa el estudio, el porcentaje de eficacia final de la vacuna puede variar. El DMC no ha informado ningún problema de seguridad grave y recomienda que el estudio continúe recopilando datos adicionales de seguridad y eficacia según lo planeado. Los datos se discutirán con las autoridades reguladoras de todo el mundo".
"Esto significa que estamos un paso más cerca de brindarles a las personas de todo el mundo un avance muy necesario para ayudar a poner fin a esta pandemia mundial. Este es un primer paso, pero fundamental, en nuestro trabajo para ofrecer una vacuna segura y eficaz".
“Quiero agradecer a las miles de personas que se ofrecieron como voluntarias para participar en el ensayo clínico, a nuestros colaboradores académicos e investigadores en los sitios del estudio, ya nuestros colegas y colaboradores de todo el mundo que están dedicando su tiempo a este esfuerzo crucial”, agregó Bourla. "No podríamos haber llegado tan lejos sin el tremendo compromiso de todos los involucrados".
"Estimamos que tras dos meses de datos de seguridad, después de la segunda y última dosis de la vacuna candidata, requerida por la guía de la FDA para una posible autorización de uso de emergencia, estará disponible para la tercera semana de noviembre".
“El primer análisis intermedio de nuestro estudio global de fase 3 proporciona evidencia de que una vacuna puede prevenir eficazmente el COVID-19. Esta es una victoria para la innovación, la ciencia y un esfuerzo de colaboración global ”, dijo el profesor Ugur Sahin, cofundador y director ejecutivo de BioNTech.
“Cuando nos embarcamos en este viaje hace 10 meses, esto es lo que aspiramos a lograr. Especialmente hoy, mientras todos estamos en medio de una segunda ola y muchos de nosotros encerrados, apreciamos aún más lo importante que es este hito en nuestro camino para poner fin a esta pandemia y para que todos recuperemos un sentido de normalidad. Continuaremos recopilando más datos a medida que el ensayo continúe inscribiéndose para un análisis final planificado cuando se hayan acumulado un total de 164 casos confirmados de COVID-19. Me gustaría agradecer a todos los que han contribuido a hacer posible este importante logro ”.
El ensayo clínico de fase 3 de BNT162b2 comenzó el 27 de julio y ha inscrito a 43,538 participantes hasta la fecha, 38,955 de los cuales han recibido una segunda dosis de la vacuna candidata al 8 de noviembre de 2020. Aproximadamente el 42 % de los participantes globales y el 30 % de los participantes de EE.UU. tienen antecedentes raciales y étnicos diversos.
El ensayo continúa inscribiéndose y se espera que continúe hasta el análisis final cuando se hayan acumulado un total de 164 casos confirmados de COVID-19. El estudio también evaluará el potencial de la vacuna candidata para brindar protección contra COVID-19 en aquellos que han tenido una exposición previa al SARS-CoV-2, así como la prevención de la vacuna contra la enfermedad grave de COVID-19.
Además de los criterios de valoración primarios de eficacia que evalúan los casos confirmados de COVID-19 acumulados 7 días después de la segunda dosis, el análisis final ahora incluirá, con la aprobación de la FDA, nuevos criterios de valoración secundarios que evalúan la eficacia en función de los casos acumulados 14 días después de la segunda dosis. dosis también. Las empresas creen que la adición de estos criterios de valoración secundarios ayudará a alinear los datos de todos los estudios de vacunas COVID-19 y permitirá el aprendizaje cruzado y las comparaciones entre estas nuevas plataformas de vacunas. Las empresas han publicado una versión actualizada del protocolo del estudio en https://www.pfizer.com/science/coronavirus.

Albert Bourla, presidente y director ejecutivo de Pfizer, ha anunciado una gran noticia para la lucha contra la COVID-19, al compartir que el proyecto de vacuna en el que trabajan, junto con el laboratorio alemán BioNTech, ha ofrecido "resultados positivos de eficacia de nuestro estudio de fase 3, etapa tardía de nuestra posible vacuna COVID-19". “Hoy es un gran día para la ciencia y la humanidad".
“Estamos alcanzando este hito crítico en nuestro programa de desarrollo de vacunas en un momento en el que el mundo más lo necesita, con tasas de infección que establecen nuevos récords, hospitales que se acercan al exceso de capacidad y economías que luchan por reabrir. Con las noticias de hoy, estamos un paso significativo más cerca de brindar a las personas de todo el mundo un avance muy necesario para ayudar a poner fin a esta crisis de salud mundial. Esperamos poder compartir datos adicionales de eficacia y seguridad generados por miles de participantes en las próximas semanas ”. D
Esta candidata a vacuna supera el 90% de efectividad para prevenir COVID-19 en participantes sin evidencia de infección previa por SARS-CoV-2, "en el primer análisis de eficacia provisional". "Los resultados demuestran que nuestra vacuna basada en ARNm puede ayudar a prevenir COVID-19 en la mayoría de las personas que la reciben".
"La división de casos entre las personas vacunadas y las que recibieron el placebo indica una tasa de eficacia de la vacuna superior al 90 %, 7 días después de la segunda dosis. Esto significa que la protección se logra 28 días después del inicio de la vacunación, que consiste en un esquema de 2 dosis. A medida que continúa el estudio, el porcentaje de eficacia final de la vacuna puede variar. El DMC no ha informado ningún problema de seguridad grave y recomienda que el estudio continúe recopilando datos adicionales de seguridad y eficacia según lo planeado. Los datos se discutirán con las autoridades reguladoras de todo el mundo".
"Esto significa que estamos un paso más cerca de brindarles a las personas de todo el mundo un avance muy necesario para ayudar a poner fin a esta pandemia mundial. Este es un primer paso, pero fundamental, en nuestro trabajo para ofrecer una vacuna segura y eficaz".
“Quiero agradecer a las miles de personas que se ofrecieron como voluntarias para participar en el ensayo clínico, a nuestros colaboradores académicos e investigadores en los sitios del estudio, ya nuestros colegas y colaboradores de todo el mundo que están dedicando su tiempo a este esfuerzo crucial”, agregó Bourla. "No podríamos haber llegado tan lejos sin el tremendo compromiso de todos los involucrados".
"Estimamos que tras dos meses de datos de seguridad, después de la segunda y última dosis de la vacuna candidata, requerida por la guía de la FDA para una posible autorización de uso de emergencia, estará disponible para la tercera semana de noviembre".
“El primer análisis intermedio de nuestro estudio global de fase 3 proporciona evidencia de que una vacuna puede prevenir eficazmente el COVID-19. Esta es una victoria para la innovación, la ciencia y un esfuerzo de colaboración global ”, dijo el profesor Ugur Sahin, cofundador y director ejecutivo de BioNTech.
“Cuando nos embarcamos en este viaje hace 10 meses, esto es lo que aspiramos a lograr. Especialmente hoy, mientras todos estamos en medio de una segunda ola y muchos de nosotros encerrados, apreciamos aún más lo importante que es este hito en nuestro camino para poner fin a esta pandemia y para que todos recuperemos un sentido de normalidad. Continuaremos recopilando más datos a medida que el ensayo continúe inscribiéndose para un análisis final planificado cuando se hayan acumulado un total de 164 casos confirmados de COVID-19. Me gustaría agradecer a todos los que han contribuido a hacer posible este importante logro ”.
El ensayo clínico de fase 3 de BNT162b2 comenzó el 27 de julio y ha inscrito a 43,538 participantes hasta la fecha, 38,955 de los cuales han recibido una segunda dosis de la vacuna candidata al 8 de noviembre de 2020. Aproximadamente el 42 % de los participantes globales y el 30 % de los participantes de EE.UU. tienen antecedentes raciales y étnicos diversos.
El ensayo continúa inscribiéndose y se espera que continúe hasta el análisis final cuando se hayan acumulado un total de 164 casos confirmados de COVID-19. El estudio también evaluará el potencial de la vacuna candidata para brindar protección contra COVID-19 en aquellos que han tenido una exposición previa al SARS-CoV-2, así como la prevención de la vacuna contra la enfermedad grave de COVID-19.
Además de los criterios de valoración primarios de eficacia que evalúan los casos confirmados de COVID-19 acumulados 7 días después de la segunda dosis, el análisis final ahora incluirá, con la aprobación de la FDA, nuevos criterios de valoración secundarios que evalúan la eficacia en función de los casos acumulados 14 días después de la segunda dosis. dosis también. Las empresas creen que la adición de estos criterios de valoración secundarios ayudará a alinear los datos de todos los estudios de vacunas COVID-19 y permitirá el aprendizaje cruzado y las comparaciones entre estas nuevas plataformas de vacunas. Las empresas han publicado una versión actualizada del protocolo del estudio en https://www.pfizer.com/science/coronavirus.















Normas de participación
Esta es la opinión de los lectores, no la de este medio.
Nos reservamos el derecho a eliminar los comentarios inapropiados.
La participación implica que ha leído y acepta las Normas de Participación y Política de Privacidad
Normas de Participación
Política de privacidad
Por seguridad guardamos tu IP
216.73.216.129